全球约有近2.8亿人受抑郁症的困扰,其中中国抑郁症患者约为9500,每年有超过70万人因抑郁而选择自杀[1, 2]。目前抑郁症治疗主要包括抗抑郁药物、心理治疗以及非药物性治疗手段[3]。传统抗抑郁药物普遍存在着起效缓慢、有效率低、不良反应多及用药后复发率高等问题[2, 3]。氯胺酮具有快速抗抑郁作用,其在难治性抑郁症患者中表现尤为显著[4, 5]。但临床试验数据揭示氯胺酮在疗效和安全性方面仍然存在很大的挑战[4, 5]。因此,亟需明确抑郁障碍的关键新靶点,深入了解新靶点作用机制,并以此为基础开发首创性新型药物。
曹聪课题组前期研究发现并确立Gαi1/3(G蛋白抑制型α亚基1和3)作为抑郁障碍核心新靶点。Gαi1/3在多个抑郁模型脑组织及人脑组织中表达显著下调。小鼠海马区神经元特异性敲减(nKD)或者条件性敲除(cKO)Gαi1/3后诱导小鼠抑郁样行为[6, 7];反之,CMS模型鼠海马区注射Gαi3过表达病毒则缓解CMS小鼠抑郁样行为[6]。机制研究发现,在BDNF刺激下,Gαi1/3和TrkB互作并介导下游Akt-mTOR等信号转导;而Gαi1/3敲除、敲减显著抑制BDNF诱导的下游信号活化,海马神经元树突数目、长度及单位距离树突棘的数目亦显著下降,从而创新性地揭示了该蛋白通过介导BDNF信号转导而跨越传统GPCR信号范畴的新功能。进一步研究发现,Gαi1/3蛋白在Lys277位点的SUMO化修饰是其与TrkB受体形成信号转导复合物并激活下游Akt-mTOR通路的关键,而该修饰受线粒体蛋白RAB5IF调控的Sumo2翻译所驱动[8]。上述研究表明Gαi1/3表达与功能协同下降阻断神经元BDNF信号介导抑郁样行为。
课题组研究进一步发现突触后致密蛋白95(PSD95)是助Gαi1/3结合TrkB的关键蛋白,并基于Gαi1/3新靶点开发了First-in-class肽类化合物CN2097强化TrkB-PSD95-Gαi1/3信号抗小鼠抑郁样行为[9]。CN2097结合PSD95的PDZ结构域后易化BDNF诱导的TrkB-PSD95-Gαi1/3耦联及下游Akt-mTOR的活化[9]。腹腔注射单一剂量CN2097(10 mg/kg)能在12小时内缓解小鼠的抑郁样行为[6]。为克服CN2097亲和力较低的局限,该课题组经多年研发,基于同一靶点从百余种多肽中筛选出迭代高效多肽Syn3。低剂量的Syn3(1 mg/kg)即可显著增强BDNF信号,并快速缓解小鼠的抑郁样行为。而海马区神经元特异性敲减或敲除Gαi1/3后逆转了Syn3诱导的抗抑郁的作用[6]。

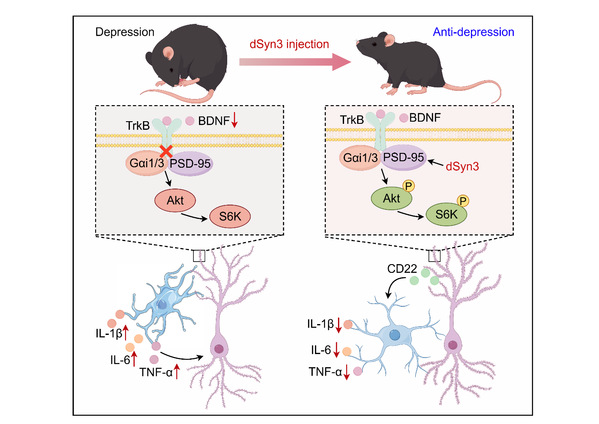
2026年4月,苏州大学曹聪课题组在Molecular Psychiatry上发表题为 “TrkB promotes the neuronal secretion of soluble Siglec-2 (CD22) to mitigate microglial activation and alleviate depression-like behaviors in male mice”的研究论文[10]。该研究以Gαi1/3新靶点开发了新型化合物dSyn3,后者通过强化BDNF信号,并诱导神经元分泌CD22以抑制小胶质细胞活化,从而协同快速长效缓解小鼠的抑郁样行为。
在基于Gαi1/3新靶点开发的Syn3的基础上,利用D型氨基酸局部替代策略开发了迭代多肽dSyn3。dSyn3与PSD95的亲和力大幅跃升,展现出更优的血脑屏障穿透力、更高的脑内峰值浓度及更长的半衰期。在体外培养的小鼠海马神经元中,添加100 nM的dSyn3显著强化BDNF诱导的下游Akt-mTOR信号活化。dSyn3还增加小鼠海马神经元的树突复杂性、树突棘的数目和突触的数量。单次注射低剂量的dSyn3(0.5 mg/kg)仅需4小时即可起效,且药效持续48小时以上。此外,dSyn3抗抑郁活性和氯胺酮相当。而海马神经元特异性敲除Gαi1/3或特异性敲减TrkB则逆转了dSyn3的抗抑郁作用。
抑郁障碍还和神经炎症微环境密切相关。小胶质细胞活化在抑郁障碍的病理中起着重要作用。机制研究创新性地发现,dSyn3在强化BDNF信号的同时,还诱导神经元分泌CD22,从而抑制小胶质细胞的活化,进一步抵抗小鼠的抑郁样行为。该研究还发现CD22是S-氯胺酮发挥抗炎作用和长效抗抑郁作用的关键靶点,海马神经元特异性敲减CD22,不影响S-氯胺酮的快速抗抑郁作用,但阻断了其长效抗抑郁作用。
因此,基于课题组前期鉴定的核心新靶点Gαi1/3成功研发了具有自主知识产权的迭代式First-in-class肽类药物,实现了从CN2097到Syn3再到高效迭代多肽dSyn3的性能跨越。dSyn3不仅表现出极高的靶点亲和力和较强的血脑屏障穿透能力,创新性地实现了“强化BDNF营养信号”与“抑制小胶质细胞活化”的双重协同作用;而且在低剂量下(0.5 mg/kg)dSyn3即可于4小时内快速起效并维持长效抗抑郁效应。该研究为基于新靶点的快速起效抗抑郁药物研发提供了具有高度原创性与临床转化潜力的先导化合物。
论文链接:https://www.nature.com/articles/s41380-026-03575-7
参考文献:
[1] W. Marx, B. Penninx, M. Solmi, T.A. Furukawa, J. Firth, A.F. Carvalho, M. Berk, Major depressive disorder, Nat Rev Dis Primers 9(1) (2023) 44.
[2] S. Marwaha, E. Palmer, T. Suppes, E. Cons, A.H. Young, R. Upthegrove, Novel and emerging treatments for major depression, Lancet 401(10371) (2023) 141-153.
[3] G.S. Malhi, J.J. Mann, Depression, Lancet 392(10161) (2018) 2299-2312.
[4] C. Liao, A.N. Dua, C. Wojtasiewicz, C. Liston, A.C. Kwan, Structural neural plasticity evoked by rapid-acting antidepressant interventions, Nat Rev Neurosci 26(2) (2025) 101-114.
[5] S.Y. Smith-Apeldoorn, J.K. Veraart, J. Spijker, J. Kamphuis, R.A. Schoevers, Maintenance ketamine treatment for depression: a systematic review of efficacy, safety, and tolerability, Lancet Psychiatry 9(11) (2022) 907-921.
[6] X. Shi, X.Z. Zhou, G. Chen, W.F. Luo, C. Zhou, T.J. He, M.T. Naik, Q. Jiang, J. Marshall, C. Cao, Targeting the postsynaptic scaffolding protein PSD-95 enhances BDNF signaling to mitigate depression-like behaviors in mice, Sci Signal 17(834) (2024) eadn4556.
[7] J. Marshall, X.Z. Zhou, G. Chen, S.Q. Yang, Y. Li, Y. Wang, Z.Q. Zhang, Q. Jiang, L. Birnbaumer, C. Cao, Antidepression action of BDNF requires and is mimicked by Galphai1/3 expression in the hippocampus, Proc Natl Acad Sci U S A 115(15) (2018) E3549-E3558.
[8] X. Shi, H.Q. Liu, S.Z. Cai, Y.H. Shen, J.L. Chai, M.Q. Zhang, C.Y. Xu, Z.Q. Zhang, J. Marshall, C. Cao, The protein RAB5IF promotes BDNF signaling by stimulating the SUMOylation of Galpha(i1/3) to reduce depressive-like behaviors in mice, Sci Signal 19(931) (2026) eaec8898.
[9] C. Cao, M.S. Rioult-Pedotti, P. Migani, C.J. Yu, R. Tiwari, K. Parang, M.R. Spaller, D.J. Goebel, J. Marshall, Impairment of TrkB-PSD-95 signaling in Angelman syndrome, PLoS Biol 11(2) (2013) e1001478.
[10] X. Shi, S.Z. Cai, J.L. Chai, C.Y. Xu, B.Y. Zhou, H.Q. Liu, J. Marshall, C. Cao, TrkB promotes the neuronal secretion of soluble Siglec-2 (CD22) to mitigate microglial activation and alleviate depression-like behaviors in male mice, Mol Psychiatry (2026).
